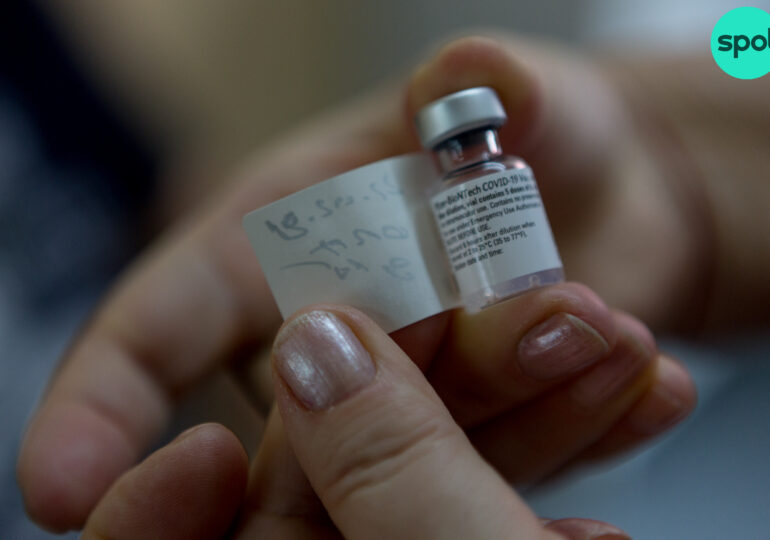
Agenţia Europeană pentru Medicamente (EMA) se va pronunţa vineri în privinţa autorizării vaccinului Pfizer-BioNTech pentru tinerii cu vârste cuprinse între 12 şi 15 ani, au anunţat reprezentanţii acestei autorităţi de reglementare.
Dacă va fi aprobat, serul Pfizer va deveni primul vaccin autorizat de EMA pentru a fi administrat adolescenţilor din cele 27 de ţări al Uniunii Europene. Pentru moment, acest vaccin este autorizat doar pentru persoanele de peste 16 ani.
EMA va organiza vineri o conferinţă de presă pentru a prezenta "concluziile unei reuniuni extraordinare a comitetului său de evaluare a medicamentelor de uz uman (…) în legătură cu indicaţiile pediatrice ale vaccinului Comirnaty", a anunţat agenţia într-un comunicat publicat miercuri și citat de AFP.
Comirnaty este denumirea comercială a vaccinului anti-COVID-19 dezvoltat de gigantul farmaceutic american Pfizer în colaborare cu compania germană BioNTech.
Agenţia pentru alimente şi medicamente (FDA) din Statele Unite a autorizat deja vaccinul Pfizer pentru adolescenţii din grupa de vârstă de 12-15 ani.
Emer Cooke, care ocupă funcţia de director executiv al EMA, a anunţat la începutul lunii mai că agenţia europeană, al cărei sediu se află la Amsterdam, urma să realizeze o evaluare accelerată a datelor transmise de dezvoltatorii vaccinului în vederea autorizării sale pentru grupa de vârstă de 12-15 ani. Rezultatele acelei evaluări erau aşteptate iniţial în luna iunie.
Emer Cooke a declarat pe 11 mai pentru mai multe cotidiane europene că EMA a primit datele de la Pfizer-BioNTech şi că agenţia - care aştepta totodată "datele studiilor clinice şi ale unui studiu desfăşurat în Canada" - prevedea "accelerarea" procedurii sale de evaluare.
Citește articolele zilei pe SpotMedia.ro:
 Statul deschide ușile RA-APPS: Vom afla cine locuiește în vilele de protocol și ce mașini deține regia
Statul deschide ușile RA-APPS: Vom afla cine locuiește în vilele de protocol și ce mașini deține regia Nicușor Dan a convocat instituțiile de apărare la Constanța după explozia dronei din port: Trebuie să vedem ce lipsuri avem
Nicușor Dan a convocat instituțiile de apărare la Constanța după explozia dronei din port: Trebuie să vedem ce lipsuri avem Iranul pune condiții pentru pace: cere deblocarea a 24 de miliarde de dolari și avertizează că războiul s-ar putea extinde dincolo de Golful Persic
Iranul pune condiții pentru pace: cere deblocarea a 24 de miliarde de dolari și avertizează că războiul s-ar putea extinde dincolo de Golful Persic Boris Becker, comparație între Simona Halep și Sorana Cîrstea: Ce a remarcat fostul mare campion
Boris Becker, comparație între Simona Halep și Sorana Cîrstea: Ce a remarcat fostul mare campion