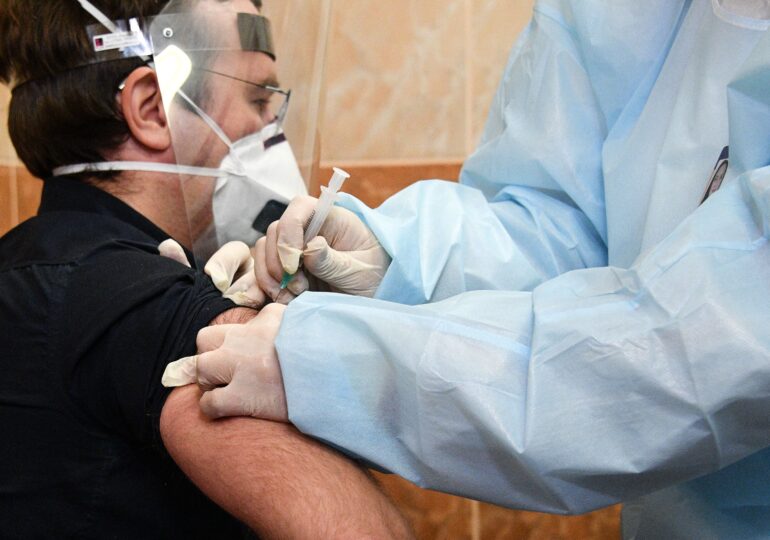
Zeci de companii, de la startup-uri din domeniul biotehnologiei până la Big Pharma, se întrec în cursa pentru un vaccin sigur şi eficient împotriva COVID-19, pentru că lumea are nevoie de un astfel de vaccin dar şi pentru profitul potenţial pe care un astfel de vaccin ar putea să-l aducă.
AFP a făcut luni o amplă analiză o actualizată a situaţiei din această cursă pentru obţinerea unui ”proiectil” magic împotriva coronavirusului care a ucis deja peste 1 milion de oameni în întreaga lume.
Câte vaccinuri sunt în pregătire?
Organizaţia Mondială a Sănătăţii (OMS) a identificat 42 de "vaccinuri candidate" în stadiul testelor clinice, faţă de 11 câte erau la jumătatea lunii iunie.
Zece dintre ele se află în cel mai avansat punct din "faza 3" de testare, punct în care este verificată eficacitatea vaccinului la scară largă, în general pe zeci de mii de persoane de pe mai multe continente.
Compania americană de biotehnologie Moderna, o colaborare americano-germană între BioNTech şi Pfizer, câteva laboratoare farmaceutice chineze controlate de stat şi un proiect european coordonat de Universitatea Oxford şi de compania AstraZeneca se numără printre cei mai promiţători actori implicaţi în cursa pentru vaccin.
Ce fel de vaccinuri?
Unele metode pentru obţinerea unui vaccin sunt deja încercate şi verificate în timp, iar altele rămân experimentale.
Vaccinurile "clasice" inactivate folosesc un corpuscul viral ce a fost inactivat, "mort", în timp ce altele folosesc tulpini virale slăbite sau "atenuate" care sunt totuşi suficient de virulente pentru a declanşa producţia de anticorpi, dar fără să provoace îmbolnăviri.
Aşa-numitele vaccinuri "sub-unitare" conţin un fragment derivat din agentul patogen pentru a produce un răspuns imunitar corespunzător.
Varietăţile de tip "vector viral" folosesc alte forme de virus "viu" pentru a transmite ADN în celulele umane, declanşând un răspuns imunitar. Spre exemplu, un virus al pojarului, modificat cu o proteină specifică noului coronavirus poate fi folosit împotriva COVID-19.
Există şi vaccinuri experimentale bazate pe gene, care folosesc fragmente ADN sau ARN.
Care sunt rezultatele?
Până în prezent, doar rezultatele testelor din fazele 1 şi 2 au fost publicate în reviste şi jurnale medicale în regim peer-review.
Vineri, rezultatele preliminare care arată că vaccinul dezvoltat de compania chineză Sinopharm induce un răspuns imunitar au fost publicate în The Lancet.
Studii similare au prezentat în ultimele săptămâni stadiul de dezvoltare al unuia dintre vaccinurile ruseşti, precum şi pe cel al vaccinului de la Universitatea Oxford, al vaccinului creat de compania chineză CanSino şi al celui de la Moderna.
Deşi rezultatele preliminare sunt încurajatoare, este prea devreme pentru a şti dacă aceste vaccinuri vor fi un succes. Testele pentru două vaccinuri candidat - produse de Johnson & Johnson şi Eli Lilly - au fost, recent, oprite temporar din cauza unor îngrijorări legate de siguranţă.
Însă acest lucru nu este neapărat o veste proastă, susţine Stephen Evans, profesor de farmacoepidemiologie la London School of Hygiene and Tropical Medicine.
"Faptul că aceste teste au fost oprite temporar arată că trebuie să existe încredere că întregul proces de monitorizare a siguranţei participanţilor la teste funcţionează corespunzător", a susţinut el.
Cazuri recente, în care pacienţi vindecaţi de COVID-19 s-au infectat pentru a doua oară cu o nouă tulpină, ridică întrebări cu privire la perioada de timp în care cei vaccinaţi vor fi şi protejaţi.
Viteză vs. siguranţă
Companii susţinute de guvernele din China, Rusia şi SUA se întrec să fie primele care trec linia de sosire.
La începutul lunii august preşedintele rus Vladimir Putin a proclamat victoria, anunţând vaccinul Sputnik V înainte ca faza a 3-a de testare să înceapă. Însă puţini din afara Rusiei au acceptat să încerce acest vaccin, iar experţii au considerat că anunţul făcut de Putin a fost prematur.
Donald Trump a promis un vaccin înainte de alegerile din 3 noiembrie, însă este puţin probabil că se va putea ţine de cuvânt. La începutul acestei luni, Administraţia americană pentru Alimente şi Medicamente (FDA) a anunţat că va avea nevoie de datele adunate timp de până la 2 luni după actul vaccinării înainte de a elibera o autorizaţie de urgenţă pentru folosirea unui vaccin.
Iar vineri, Pfizer a anunţat că vaccinul său nu va fi gata până la jumătatea lui noiembrie.
"Ceea ce este diferit pentru vaccinurile împotriva COVID-19 este că viteza de dezvoltare şi de obţinere a aprobării potenţiale este mult mai mare din cauza urgenţei de sănătate publică", a notat Agenţia Europeană pentru Medicamente. Însă nici măcar această nevoie stringentă nu poate fi folosită pentru a invoca trecerea peste reguli.
"Înainte de aprobare, toate vaccinurile din Uniunea Europeană sunt evaluate la aceleaşi standarde ridicate la fel ca şi orice alte medicamente", conform unui comunicat al Agenţiei Europene pentru medicamente.
Citește și:
 Astronomii au găsit rămășițele unei galaxii primitive înghițite de Calea Lactee
Astronomii au găsit rămășițele unei galaxii primitive înghițite de Calea Lactee Bolojan revine asupra scandalului reactoarelor de la Doicești: Proiectul are niște probleme pe care nu le putem nega
Bolojan revine asupra scandalului reactoarelor de la Doicești: Proiectul are niște probleme pe care nu le putem nega Iranul anunță că analizează o nouă ofertă de pace, Trump spune că negocierile sunt ”pe muchie de cuțit”
Iranul anunță că analizează o nouă ofertă de pace, Trump spune că negocierile sunt ”pe muchie de cuțit” Jaqueline Cristian, eliminată în semifinale la Strasbourg
Jaqueline Cristian, eliminată în semifinale la Strasbourg